科研:水质 亚硝胺的测定 液液萃取-气相色谱法
警告!亚硝胺是致癌物,其标准物质和标准贮备液在使用过程中,避免接触皮肤、眼睛等;应在通风良好的室内通风橱中进行试验操作;使用二氯甲烷、乙醚、戊烷等试剂时,应佩戴防护器具,避免吸入或接触皮肤和衣物。
1、适用范围
本标准规定了水中亚硝胺的液液萃取-气相色谱法。
本标准适用于地表水、地下水、工业废水和生活污水中N-亚硝基二甲胺、N-亚硝基二乙胺、N-亚硝基二正丙胺和N-亚硝基二苯胺的测定。
当取样量为250ml时,本方法的检出限分别为:N-亚硝基二甲胺0.86μg/L、N-亚硝基二乙胺0.78μg/L、N-亚硝基二正丙胺0.65μg/L、N-亚硝基二苯胺0.96μg/L;测定下限分别为:N-亚硝基二甲胺3.4μg/L、N-亚硝基二乙胺3.1μg/L、N-亚硝基二正丙胺2.6μg/L、N亚硝基二苯胺3.8μg/L。
2、规范性引用文件
本标准内容引用了下列文件中的条款。凡是不注日期的引用文件,其有效版本适用于本标准。
HJ/T91地表水和污水监测技术规范
HJ/T164地下水环境监测技术规范
3、方法原理
用二氯甲烷萃取水样中的亚硝胺,经无水硫酸钠脱水、浓缩,弗罗里硅土柱或碱性氧化铝柱净化后,用氮吹仪浓缩定容。采用带氢火焰离子检测器(FID)的气相色谱仪进行分析,根据保留时间进行定性,峰面积(或峰高)定量。
4、试剂和材料
除非另有说明,分析时均使用符合国家标准的分析纯化学试剂,实验室用水为新制备的去离子水或蒸馏水。
4.1 二氯甲烷、甲醇、丙酮和戊烷:色谱纯或相当纯度
在色谱分析条件下无干扰峰出现,否则应用全玻璃容器进行重蒸馏。
4.2 乙醚
应通过过氧化物试纸指示是否存在过氧化物。如果存在过氧化物需要在全玻璃容器中重蒸馏。然后,在每1L乙醚中应加入20ml乙醇作为保护剂。
4.3 硫代硫酸钠(Na2S2O3):优级纯。
4.4 无水硫酸钠(Na2SO4):优级纯
使用前在450℃烘箱中烘烤4h,置于干燥器中冷却至室温,贮存在密封玻璃瓶中。
4.5 弗罗里硅土(Florisil):PR级(60~100目)
在650℃下,烘5h并贮存于具玻璃塞或内衬铝箔的螺旋盖棕色玻璃容器内。使用前,在衬有铝箔的玻璃容器中于130℃活化16h。
4.6 碱性氧化铝
把l00g氧化铝放入50ml试剂瓶中,加入2ml水,振荡,充分混合10min。贮存于具玻璃塞或内衬铝箔的螺旋盖棕色玻璃容器中,放置至少2h后使用。
4.7 玻璃棉:市售经硅烷化处理的玻璃棉(使其呈惰性,去除与样品接触中表现的活性)。
4.8 氢氧化钠溶液:c(NaOH)=10mol/L
准确称取40.0g氢氧化钠溶于适量水中,待冷却后转移至100ml容量瓶,加水稀释至标线,混匀。
4.9 硫酸溶液:1+1。
4.10 色谱标准贮备液:ρ=2000mg/L
分别准确称取N-亚硝基二甲胺、N-亚硝基二乙胺、N-亚硝基二正丙胺和N-亚硝基二苯胺各0.0200g于10ml容量瓶中,用甲醇定容至10ml刻度。或购买市售有证标准物质。
4.11 色谱标准使用液:ρ=200mg/L
分别准确量取1.00ml标准贮备液(4.10)于10ml容量瓶中,用甲醇定容至10ml刻度。
4.12 氮气:纯度≥99.99%。
4.13 氢气:纯度≥99.99%。
5 仪器和设备
5.1 气相色谱仪:具氢火焰离子化检测器(FID)。
5.2 色谱柱:5%苯基,95%二甲基硅氧烷非极性毛细管柱等,或其他等效色谱柱。
5.3 采样瓶:500ml、1000ml具塞磨口玻璃瓶。
5.4 旋转蒸发装置或自动浓缩仪。
5.5 氮吹浓缩仪。
5.6 分析天平:精度为0.0001g。
5.7 全玻璃蒸馏装置:500ml蒸馏瓶及与之配套的冷凝管和磨口弯管接口。
5.8 微量注射器:1μl、10μl、50μl。
5.9 棕色样品瓶:1.5ml,带聚四氟乙烯衬里密封螺旋盖。
5.10 层析柱Ⅰ:大约400mm长×22mm内径,用于弗罗里硅土柱净化法。
5.11 层析柱Ⅱ:大约300mm长×10mm内径,用于碱性氧化铝柱净化法。
5.12 无水硫酸钠干燥柱:内径0.6~0.8cm,带活塞玻璃柱,内装填2g无水硫酸钠,柱下端用玻璃棉固定。
5.13 分液漏斗:500ml。
5.14 一般实验室常用仪器设备。
6 样品
6.1 样品的采集和保存
参照HJ/91和HJ/T164的相关规定进行水样的采集和保存。
使用采样瓶(5.3)采集水样,水样要完全注满采样瓶,不留气泡。分析前用氢氧化钠溶液(4.8)或硫酸溶液(4.9)调节样品的pH值为6~9。若水中有残余的氯存在,要在每升样品要加入80mg硫代硫酸钠(4.3)除氯。
亚硝胺在水中不够稳定,样品应在避光低温环境(4℃以下)保存和运输,7天内萃取,萃取后40天内完成分析。
6.2 试样的制备
6.2.1 萃取和浓缩
6.2.1.1 摇匀水样,准确量取250ml水样于500ml分液漏斗(5.13)中,加入50ml二氯甲烷(4.1),振荡萃取2min,静置10min,两相分层,收集有机相于250ml锥形瓶中,重复萃取两遍。合并有机相,并通过无水硫酸钠柱(5.12)脱水,收集洗脱液于旋转瓶中,再用10ml二氯甲烷洗脱无水硫酸钠柱,并收集洗脱液。
6.2.1.2 使用旋转蒸发仪在加热温度40℃、旋转速度60r/min条件下,将上述洗脱液浓缩至约5ml。
6.2.1.3 将上述浓缩过的洗脱液转移至10ml氮吹管中氮吹至约0.9ml,用带胶头的玻璃毛细管将试液移入样品瓶(5.9)中,并用二氯甲烷(4.1)定容至1ml,待净化。
注:地表水、地下水以及含亚硝胺浓度较高但成分简单的工业废水的萃取液可不经过净化,备色谱分析用。
6.2.2 净化
6.2.2.1 佛罗里硅土(Florisil)柱净化
在层析柱Ⅰ(5.10)中放入22g已经活化的佛罗里硅土(Florisil)(4.5),轻轻敲击柱子使其向下沉实,在佛罗里硅土(Florisil)层上面加入约5mm厚无水硫酸钠层。用40ml乙醚/戊烷(15+85)(v/v)预洗脱柱子,弃去洗脱液,当硫酸钠层恰好暴露到空气之前,加入旋转蒸发仪浓缩后的5ml萃取液(6.2.1.2),同时用2ml戊烷洗涤旋转瓶,一并注入完成转移。
用90ml乙醚/戊烷(15+85)(v/v)进行第一次洗脱,弃去洗脱液。然后,用100ml乙醚/戊烷(5+95)(v/v)进行第二次洗脱,收集洗脱液于另一旋转瓶中,加入15ml甲醇至旋转瓶中。使用旋转蒸发仪在加热温度40℃,旋转速度60r/min条件下,将洗脱液浓缩至约5ml,转至氮吹管中。用2ml甲醇洗涤旋转瓶并转至氮吹管中,重复两次,将所有洗脱液氮吹浓缩至0.9ml,用甲醇定容至1ml,备色谱分析用。
6.2.2.2 碱性氧化铝柱净化
在层析柱Ⅱ(5.11)中放入12g准备好的碱性氧化铝(4.6),轻轻敲击柱子让其向下沉实,在碱性氧化铝层上面加入约1~2cm厚无水硫酸钠层。用10ml乙醚/戊烷(3+7)(v/v)预洗脱柱子,弃去洗脱液,当硫酸钠层恰好暴露到空气之前,加入旋转蒸发仪浓缩后的5ml萃取液(6.2.1.2),同时用2ml戊烷洗涤旋转瓶,一并注入完成转移。
用10ml乙醚/戊烷(3+7)(v/v)进行洗脱,弃去洗脱液。然后用60ml乙醚/戊烷(1+1)(v/v)洗脱柱子,收集洗脱液于旋转瓶中,加入15ml甲醇至旋转瓶中。使用旋转蒸发仪在加热温度40℃、旋转速度60r/min条件下,将洗脱液浓缩至约 5ml,转至氮吹管中。用2ml甲醇洗涤旋转瓶并转至氮吹管中,重复两次,将所有洗脱液氮吹浓缩至0.9ml,用甲醇定容至1ml,备色谱分析用。
6.3 空白试样的制备
取250ml实验用水代替水样,按照与试样的制备(6.2)相同萃取、浓缩步骤,制备空白试样。
7 分析步骤
7.1 仪器调试
按照仪器说明书的要求进行仪器调试,本标准的推荐分析条件如下:
气化室温度:250℃;
柱温:50℃,保持2.5min,再以30/min℃升温至220℃,保持4min;
检测器温度:300℃;
分流比:1:1;
载气:氮气流量1.2ml/min;
燃气:氢气流量30ml/min;
助燃气:空气流量400ml/min。
7.2 校准
7.2.1 标准曲线的绘制
用微量注射器(5.8)分别准确移取四种亚硝胺标准使用液(4.11)5μl、10μl、20μl、30μl、40μl、50μl于1.5ml棕色样品瓶(5.9)中,分别用二氯甲烷稀释至1ml。制备6个浓度点的标准系列,各组分质量浓度分别为1mg/L、2mg/L、4mg/L、6mg/L、8mg/L、10mg/L。分别移取标准使用液1μl注入气相色谱仪,得到各不同浓度的亚硝胺色谱图。以峰高或峰面积为纵坐标,亚硝胺的质量浓度(mg/L)为横坐标,绘制标准曲线。
7.2.2 标准样品的色谱图
在本标准推荐的色谱条件下,亚硝胺的标准色谱图,见图1。
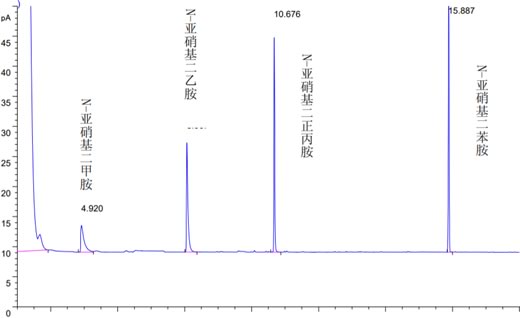
图1四种亚硝胺的标准样品色谱图(N亚硝基二甲胺 4.920、N亚硝基二乙胺 8.067、N亚硝基二正丙胺 10.676、N亚硝基二苯胺 15.887
7.3 测定
取1μl待测试样注入气相色谱仪中,按照与绘制标准曲线相同色谱分析条件进行测定。
记录色谱峰的保留时间和峰高(或峰面积)。
7.4 空白试验
在分析样品的同时,应作全程序空白试验。移取1μl空白试样,按照与样品测定相同步骤进行分析,检查分析过程中是否有污染。
8 结果计算与表示
8.1 结果计算
水样中亚硝胺各目标组分的浓度(mg/L),按照公式(1)进行计算。
ρi = V
ρχi ×V1
ρi —样品中目标组分 i 的质量浓度,mg/L;
ρχi —从标准曲线中查得目标组分 i 的质量浓度,mg/L;
V1—萃取液浓缩后的体积,ml;
V —水样的体积,ml。
8.2 结果表示
8.2.1 定性结果
根据标准物质各组分的保留时间确定被测样品中的组分及名称。
8.2.2 定量结果
根据标准曲线来计算样品中各组分的质量浓度。测定结果保留3位有效数字。
9 精密度和准确度
六家实验室分别对四种亚硝胺的3种不同浓度的实际样品进行了测定:实验室内相对标准偏差为0.36%~13.0%;实验室间相对标准偏差为8.50%~14.5%;重复性限为0.87μg/L~6.63μg/L;再现性限为2.36μg/L~14.4μg/L。
六家实验室对含四种亚硝胺浓度为2mg/L、5mg/L、10mg/L的标准样品进行测定:相对误差为0.25%~1.11%;相对误差最终值为2.24±4.36%~4.42±4.62%。
六家实验室分别对三种实际样品进行了加标分析测定,加标浓度为5mg/L,四种亚硝胺实际样品的平均加标回收率范围为57.0%~85.9%。
具体每种亚硝胺的精密度和准确度结果,参见附录A。
10 质量保证和质量控制
10.1 空白试验
每批试剂做一次试剂空白试验,试剂空白试验结果应低于方法检出限。每分析一批样品至少做一个全程序空白试验,全程序空白如有检出,应在计算结果中扣除。
10.2 校准
10.2.1 初始标准曲线的相关系数应大于等于0.999。
10.2.2 连续校准(曲线中间点检查)
每个工作日应进行一次连续校准分析。连续校准一定要在空白和样品分析之前。
连续校准的浓度为初始曲线的一个浓度点,计算连续校准结果与最近一次初始校准曲线该点浓度的百分偏差,目标化合物的百分偏差不得高于最近一次初始标准浓度的20%以上。如果连续分析几个连续校准都不能达到允许标准,应重新绘制标准曲线。
10.3 平行分析
每批样品应至少做一次平行样品分析,平行样品分析结果相对偏差要小于20%。
11 废物处理
亚硝胺属于致癌有机污染物,实验过程中所使用的标准物质和所有有机残液应严格管理,用后不能随意倾倒,应放置在适当的密闭容器中保存,妥善处理。
文章标签:水质亚硝胺气相色谱物理科学 科研 物理仪器设备应用 点评收藏分享
采购、售后(仪器设备提交仪器设备信息
"科研:水质 亚硝胺的测定 液液萃取-气相色谱法"相关
- 新版药典对纯化水 灭菌注射用水检验电导率和总有机碳的测定方法(2个
- 新版药典对纯化水、注射用水和灭菌注射用水检验新增电导率和总有碳的测定法,新增两个检测项目。没有检测电导率和总有机碳的4个后果1、不知道药品已受污染,不知道什么原因和什么时候受到污染;2、纯水系统的过虑
